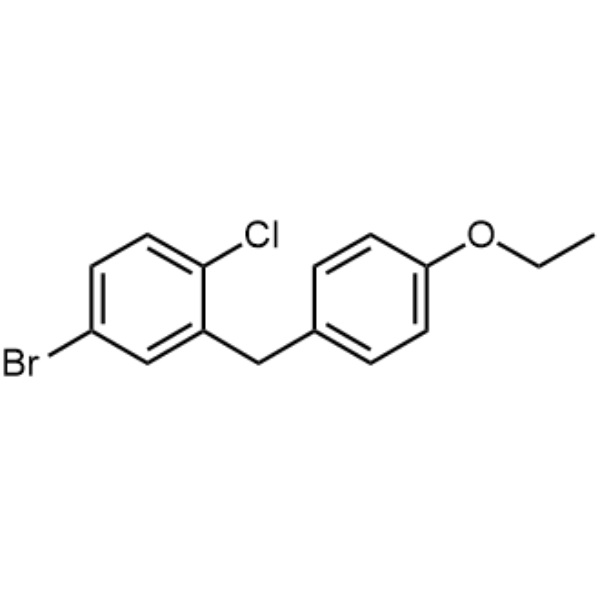
5-Bromo-2-Cloro-4′-Etoxidifenilmetano CAS 461432-23-5 Dapagliflozina Intermediário
Fornecimento do fabricante, alta pureza, produção comercial
Dapagliflozina (CAS: 461432-26-8) Intermediários relacionados:
5-Bromo-2-Ácido clorobenzóico CAS 21739-92-4
5-Bromo-2-Cloro-4'-Etoxidifenilmetano CAS 461432-23-5
2,3,4,6-Tetraquis-O-Trimetilsilil-D-Gluconolactona CAS 32384-65-9
| Nome Químico | 5-Bromo-2-Cloro-4'-Etoxidifenilmetano |
| Sinônimos | 4-Bromo-1-Cloro-2-(4-Etoxibenzil)benzeno; 4-(5-Brom-2-Clorbenzil)fenil-Éter etílico; Dapagliflozina Bromo Impureza |
| Número CAS | 461432-23-5 |
| Status do estoque | Em estoque, produção em até toneladas |
| Fórmula Molecular | C15H14BrClO |
| Peso molecular | 325,63 |
| Ponto de fusão | 41,0 a 43,0 ℃ |
| Densidade | 1,371±0,06 g/cm3 |
| COA e MSDS | Disponível |
| Local de Origem | Xangai, China |
| Marca | Ruifu Química |
| Artigo | Especificações | Resultados |
| Aparência | Pó Cristalino Branco a Pael Amarelo | Em conformidade |
| Pureza/Método de Análise | ≥98,0% (HPLC) | 98,91% |
| Água (KF) | ≤0,50% | 0,15% |
| Espectro Infravermelho | Está em conformidade com a estrutura | Em conformidade |
| Espectro de RMN de 1H | Está em conformidade com a estrutura | Em conformidade |
| Padrão de teste | Padrão Empresarial | Em conformidade |
| Aplicação | Intermediário de Dapagliflozina (CAS: 461432-26-8), diabetes tipo II | |
Pacote: Garrafa, saco de papel alumínio, tambor de papelão, 25kg/tambor ou conforme necessidade do cliente.
Condição de armazenamento:Armazenar em recipientes fechados em local fresco e seco; Proteja da luz e da umidade.

4-Bromo-1-Cloro-2-(4-Ethoxybenzyl)benzeno (CAS: 461432-23-5) é usado como intermediário na síntese de Dapagliflozina (CAS: 461432-26-8). A dapagliflozina é um potente inibidor renal seletivo do cotransportador de glicose dependente de sódio 2 (SGLT2) para o tratamento do diabetes tipo 2. A dapagliflozina é um novo medicamento antidiabético desenvolvido em conjunto pela Bristol-Myers Squibb e AstraZeneca, sendo aprovado pela Agência Europeia de Medicamentos (EMA) em 12 de novembro de 2012. Em 8 de janeiro de 2014, a Food and Drug Administration (FDA) dos EUA aprovou-o para uso no tratamento do diabetes tipo II.