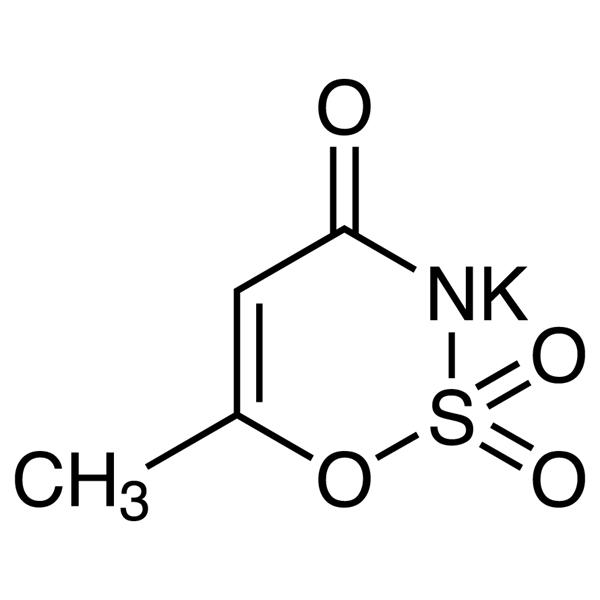
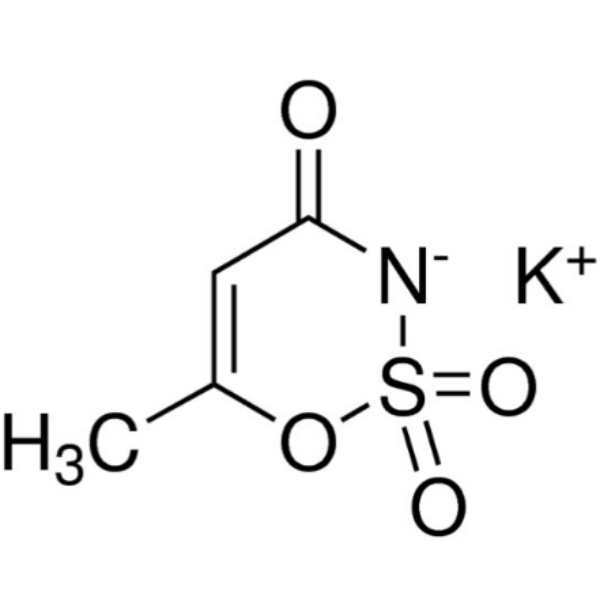
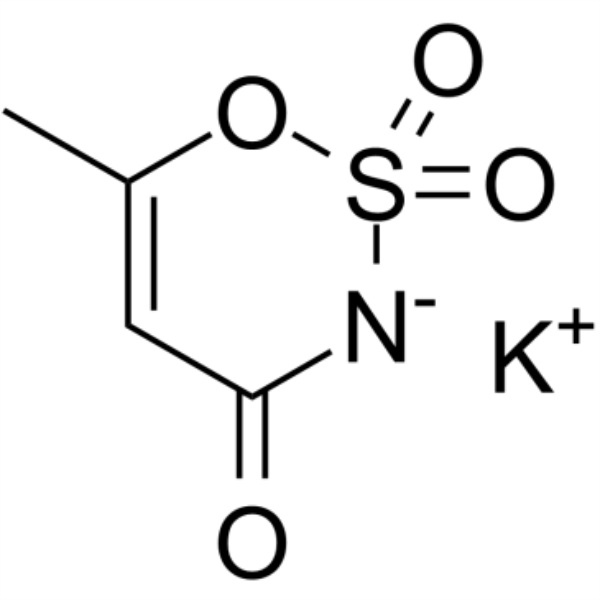
Acessulfame K CAS 55589-62-3 Acessulfame Potássio Pureza >99,0% (HPLC)
Shanghai Ruifu Chemical Co., Ltd. é o fabricante líder de acessulfame K (acessulfame de potássio) (CAS: 55589-62-3) com adoçante de ingrediente alimentar de alta qualidade. Ruifu pode fornecer entrega em todo o mundo, preços competitivos, quantidades pequenas e a granel disponíveis. Compre Acessulfame K, Entre em contato: alvin@ruifuchem.com
| Nome Químico | Acessulfame K |
| Sinônimos | Acessulfame de Potássio; Sal Acessulfame de Potássio; 6-Metil-1,2,3-Oxatiazina-4(3H)-ona 2,2-Dióxido Sal de Potássio; Potássio 6-Metil-1,2,3-Oxatiazina-4(3H)-ona 2,2-Dióxido; Otizon; Acessulfame de Potássio; Sunett; Sunnet; Doce; IDA |
| Status do estoque | Em estoque, fabricado comercialmente |
| Número CAS | 55589-62-3 |
| Fórmula Molecular | C4H4KNO4S |
| Peso molecular | 201,24 g/mol |
| Ponto de fusão | 229,0~232,0℃(dec.) |
| Sensível | Sensível à umidade |
| Solubilidade em Água | Solúvel em água, quase transparente |
| Odor | Inodoro com sabor doce |
| Temperatura de armazenamento. | Local fresco e seco (2 ~ 8 ℃, longe da umidade) |
| COA e MSDS | Disponível |
| Marca | Ruifu Química |
| Itens | Padrões de Inspeção | Resultados |
| Aparência | Pó Cristalino Branco | Cumpre |
| Conteúdo do ensaio | 99,0~101,0% (calculado com base seca) | 99,63% |
| Ponto de fusão | 229,0 ~ 232,0 ℃ | Cumpre |
| Perda na secagem | <1,00% | 0,09% |
| Cinza Sulfatada | <0,50% | Cumpre |
| Valor de pH (solução 1 em 100) | 5,5~7,5 | 6,65 |
| Potássio | 17,0~21,0% | Cumpre |
| Impurezas orgânicas | ≤20 ppm | Cumpre |
| Impureza A | ≤0,125% | Cumpre |
| Impureza B | ≤20 ppm | Cumpre |
| Metais Pesados (Pb) | ≤10ppm | <5 ppm |
| Flúor | ≤3ppm | Cumpre |
| Arsênico | ≤3ppm | Cumpre |
| Liderar | ≤1ppm | Cumpre |
| Selênio | ≤10ppm | Cumpre |
| Espectro Infravermelho | Está em conformidade com a estrutura | Cumpre |
| Espectro de RMN de 1H | Está em conformidade com a estrutura | Cumpre |
| Conclusão | O produto foi testado e está em conformidade com as especificações | |
Pacote: Garrafa, saco de folha de alumínio, tambor de 25kg/papelão, ou conforme necessidade do cliente.
Condição de armazenamento:Armazene em um recipiente bem fechado. Armazene em local fresco, seco (2 ~ 8 ℃) e bem ventilado, longe de substâncias incompatíveis. Proteja da luz e da umidade.
Envio:Entregue para todo o mundo por via aérea, pela FedEx / DHL Express. Fornece entrega rápida e confiável.
DEFINIÇÃO
Acesulfame de potássio contém NLT 99,0% e NMT 101,0% de C4H4NO4SK, calculado com base seca.
IDENTIFICAÇÃO
• A. ABSORÇÃO INFRAVERMELHA<197K>
• B. TESTES DE IDENTIFICAÇÃO-GERAL, Potássio<191>
Solução de amostra: 100 mg/mL
Critérios de aceitação: Atende aos requisitos
ENSAIO
• PROCEDIMENTO
Amostra: 150 mg
Sistema titulométrico (Ver Titrimetria<541>)
Modo: titulação direta
Titulante: ácido perclórico 0,1 N VS
Branco: 50 mL de ácido acético glacial
Detecção de endpoint: potenciométrico
Análise: Dissolver a Amostra em 50 mL de ácido acético glacial.
Titular com ácido perclórico 0,1 N VS. Execute uma determinação em branco.
Calcule a porcentagem de acessulfame de potássio (C4H4NO4SK) na amostra:
Resultado = [(V − B) × N × F × 100]/W
V = volume de titulante consumido pela amostra (mL)
B = volume de titulante consumido pelo branco (mL)
N = normalidade real do titulante (mEq/mL)
F = fator de equivalência, 201,2 mg/mEq
W = peso da amostra (mg)
Critérios de aceitação: 99,0%–101,0% na base seca
IMPUREZAS
• LIMITE DE FLUORETO
[NOTA-Use materiais plásticos durante este teste.]
Solução A: Dissolva 210 g de ácido cítrico monohidratado em 400 mL de água. Ajustar com amônia concentrada para pH 7,0 e diluir com água até 1000 mL.
Solução B: 132 mg/mL de fosfato de amônio dibásico
Solução C: A uma suspensão de 292 g de ácido edético em 500 mL de água, adicionar 200 mL de hidróxido de amônio, ajustar com hidróxido de amônio para um pH entre 6 e 7 e diluir com água para perfazer 1000 mL.
Solução tampão: Misture volumes iguais de Solução A, Solução B e Solução C e ajuste com hidróxido de amônio até um pH de 7,5.
Solução estoque padrão: Pesar 0,442 g de fluoreto de sódio, previamente seco a 300° por 12 h, em um balão volumétrico de 1-L e diluir com água até o volume. Armazene a solução em um recipiente plástico fechado. Imediatamente antes do uso, pipetar 5 mL desta solução para um balão volumétrico de 100 mL e diluir com água até o volume. Cada mL desta solução contém 10 µg de íon flúor.
Solução padrão A: Misture 0,5 mL de solução estoque padrão e 15,0 mL de solução tampão e dilua com água até 50 mL.
Solução padrão B: Misture 1,0 mL de solução estoque padrão e 15,0 mL de solução tampão e dilua com água até 50mL.
Solução padrão C: Misture 1,5 mL de solução estoque padrão e 15,0 mL de solução tampão e dilua com água até 50mL.
Solução padrão D: Misture 3,0 mL de solução estoque padrão e 15,0 mL de solução tampão e dilua com água até 50mL.
Solução amostra: Em um balão volumétrico de 50 mL adicionar 3 g de Acessulfame de Potássio. Dissolver em água, adicionar 15,0 mL de solução tampão e diluir com água até o volume.
Análise
Amostras: Solução padrão A, Solução padrão B, Solução padrão C, Solução padrão D e Solução de amostra
Medir concomitantemente o potencial (ver Titrimetria<541>) em mV, das soluções padrão e da solução amostra, com um medidor de pH adequado equipado com um eletrodo de especificação de fluoreto e um eletrodo de referência de prata-cloreto de prata. Ao realizar as medições, transfira a solução para um béquer de 25 mL e mergulhe os eletrodos. Insira uma barra de agitação revestida com poliéster no béquer, coloque o béquer em um agitador magnético com topo isolado e deixe agitar até atingir o equilíbrio (1-2 min). Enxágue e seque os eletrodos entre as medições, tomando cuidado para não riscar o cristal no eletrodo de íon específico de flúor. Meça o potencial de cada solução padrão e represente graficamente a concentração de flúor, em µg/mL, versus o potencial, em mV, em papel semilogarítmico. Meça o potencial da solução amostra e determine a concentração de flúor a partir da curva padrão, em µg/mL.
Calcule o teor, em ppm, de flúor na porção de Acessulfame de Potássio tomada:
Resultado = (V × C/W)
V = volume da solução amostra (mL)
C = concentração de flúor na solução amostra, da curva padrão (mg/mL)
W = peso de acessulfame de potássio utilizado para preparar a solução amostral (g)
Critérios de aceitação: NMT 3 ppm
• METAIS PESADOS, Método I<231>: NMT 10 ppm
• PUREZA CROMATOGRÁFICA
Solução A: 3,3 mg/mL de hidrogenossulfato de tetrabutilamônio
Fase móvel: Acetonitrila e Solução A (2:3)
Solução de adequação do sistema: 2 µg/mL de acessulfame de potássio RS da USP e etilparabeno de cada um
Solução padrão: 0,2 µg/mL de Acessulfame de Potássio RS da USP
Solução de amostra: 10 mg/mL
Sistema cromatográfico
(Ver Cromatografia<621>, Adequação do Sistema.)
Modo: LC
Detector: UV 227nm
Coluna: 4,6-mm × 25-cm; Embalagem L1 de 5-µm
Taxa de fluxo: 1 mL/min
Tamanho da injeção: 20 μL
Adequação do sistema
Amostra: Solução de adequação do sistema
Requisitos de adequação
Resolução: NLT 2 entre acessulfame de potássio e etilparabeno
Análise
Amostras: solução padrão e solução amostral
Registre os cromatogramas para um tempo de execução NLT 3 vezes o tempo de retenção do pico de acessulfame de potássio e meça as respostas de área dos picos.
Critérios de aceitação: A resposta de qualquer pico em um tempo de retenção diferente do do acessulfame de potássio da solução amostra não excede a resposta do pico do acessulfame de potássio da solução padrão (0,002%).
TESTES ESPECÍFICOS
• ACIDEZ OU ALCALINIDADE
Solução amostra: 4,0 g em 20 mL de dióxido de carbono-água livre
Análise: Adicionar 0,1 mL de azul de bromotimol TS. Se a solução for amarela, titule com hidróxido de sódio 0,01 N para produzir uma cor azul. Se a solução for azul, titule com ácido clorídrico 0,01 N para produzir uma cor amarela.
Critérios de aceitação: É necessário NMT 0,2 mL de hidróxido de sódio 0,01 N ou NMT 0,2 mL de ácido clorídrico 0,01 N.
• PERDA NA SECAGEM<731>: Secar uma amostra a 105° por 3 h: ela perde NMT 1,0% do seu peso.
REQUISITOS ADICIONAIS
• EMBALAGEM E ARMAZENAGEM: Conservar em recipiente bem fechado e proteger da luz. Armazene em temperatura ambiente.
PADRÕES DE REFERÊNCIA USP<11>
USP Acessulfame Potássio RS
Como comprar? Entre em contatoAlvin Huang: sales@ruifuchem.com ou alvin@ruifuchem.com
15 anos de experiência?Temos mais de 15 anos de experiência na fabricação e exportação de uma ampla variedade de intermediários farmacêuticos ou produtos químicos finos de alta qualidade.
Principais mercados? Vender para o mercado interno, América do Norte, Europa, Índia, Coréia, Japão, Austrália, etc.
Vantagens? Qualidade superior, preço acessível, serviços profissionais e suporte técnico, entrega rápida.
Qualidade Garantia? Sistema de controle de qualidade rigoroso. Equipamentos profissionais para análise incluem NMR, LC - MS, GC, HPLC, ICP - MS, UV, IR, OR, K.F, ROI, LOD, MP, Claridade, Solubilidade, teste de limite microbiano, etc.
Amostras? A maioria dos produtos fornece amostras grátis para avaliação de qualidade. O custo de envio deve ser pago pelos clientes.
Auditoria de Fábrica? Auditoria de fábrica bem-vinda. Por favor, marque uma consulta com antecedência.
Quantidade mínima? Sem quantidade mínima. Pedidos pequenos são aceitáveis.
Prazo de entrega? Se estiver em estoque, entrega garantida em três dias.
Transporte? Por expresso (FedEx, DHL), por via aérea, por via marítima.
Documentos? Serviço pós-venda: COA, MOA, ROS, MSDS, etc.
Síntese Personalizada? Pode fornecer serviços de síntese personalizados para melhor atender às suas necessidades de pesquisa.
Condições de pagamento? A fatura pró-forma será enviada primeiro após a confirmação do pedido, juntamente com nossos dados bancários. Pagamento por T/T (Transferência Telex), PayPal, Western Union, etc.
Códigos de risco 36/37/38 - Irritante para os olhos, vias respiratórias e pele.
Descrição de segurança
S26 - Em caso de contato com os olhos, lavar imediatamente com água em abundância e consultar um médico.
S36/37/39 - Use roupas de proteção, luvas e proteção para os olhos/face adequados.
GTK Alemanha 1
RTECS RP4489165
Código HS 2934990002
Toxicidade LD50 em ratos (mg/kg): 7.431 por via oral, 2.243 i.p. (Mayer, Kemper)
1976, Acesulfame - K foi sintetizado pela primeira vez
1983, a UE aprovou seu uso em alimentos e bebidas
1988, a FDA aprovou seu uso em adoçantes de mesa, gomas e café
1992, a China aprovou seu uso em alimentos e bebidas
1994, a FDA aprovou seu uso em xaropes, panificação e laticínios
1995, a FDA aprovou seu uso em bebidas alcoólicas
1998, a FDA aprovou seu uso em refrigerantes
2000, o Japão aprovou seu uso
Acesulfame K (acessulfame de potássio) (CAS: 55589-62-3) é um adoçante artificial.
Como adoçantes não nutritivos, não há essencialmente nenhuma alteração na concentração dos alimentos e bebidas utilizados na faixa geral de pH.
As aplicações comuns do Acesulfame - K são usos em mesa, gomas de mascar, bebidas, alimentos, produtos de panificação, confeitaria, produtos de higiene bucal e produtos farmacêuticos.
Adoçantes. Após a ingestão pelo corpo humano não é absorvido, não produz calor, adequado para uso em pacientes com diabetes e obesidade. Pode ser usado sozinho ou em combinação com outros adoçantes. O acessulfame K é frequentemente misturado com outros adoçantes (geralmente Sucralose ou Aspartame). Estas misturas têm a reputação de proporcionar um sabor mais semelhante ao da sacarose, pelo que cada adoçante mascara o sabor residual do outro e/ou exibe um efeito sinérgico pelo qual a mistura é mais doce do que os seus componentes.
Ao contrário do Aspartame, o Acesulfame K é estável ao calor, mesmo sob condições moderadamente ácidas ou básicas, permitindo que seja utilizado como aditivo alimentar na panificação ou em produtos que requerem um longo prazo de validade. Nas bebidas carbonatadas, é quase sempre utilizado em conjunto com outro adoçante, como Aspartame ou Sucralose. Também é utilizado como adoçante em shakes de proteína e produtos farmacêuticos, principalmente medicamentos mastigáveis e líquidos, onde pode tornar os princípios ativos mais palatáveis.
O acessulfame de potássio é usado como agente adoçante intenso em cosméticos, alimentos, bebidas, adoçantes de mesa, vitaminas e preparações farmacêuticas, incluindo misturas em pó, comprimidos e produtos líquidos. É amplamente utilizado como substituto do açúcar em formulações compostas e como adoçante de pasta de dente. O poder adoçante aproximado é 180-200 vezes maior que o da sacarose, semelhante ao aspartame, cerca de um terço mais doce que a sucralose, metade tão doce quanto a sacarina sódica e cerca de 4 a 5 vezes mais doce que o ciclamato de sódio.
O acessulfame de potássio é amplamente utilizado em bebidas, cosméticos, alimentos e formulações farmacêuticas e é geralmente considerado um material relativamente não tóxico e não irritante. Estudos farmacocinéticos demonstraram que o acessulfame de potássio não é metabolizado e é rapidamente excretado inalterado na urina. Estudos de alimentação de longo prazo em ratos e cães não mostraram evidências que sugiram que o acessulfame de potássio seja mutagênico ou carcinogênico.
A OMS estabeleceu uma ingestão diária aceitável de acessulfame de potássio de até 15 mg/kg de peso corporal. O Comité Científico dos Alimentos da União Europeia estabeleceu um valor de ingestão diária de até 9 mg/kg de peso corporal.
LD50 (rato, IP): 2,2 g/kg
LD50 (rato, oral): 6,9–8,0 g/kg
Acesulfame de potássio possui boa estabilidade. Na forma a granel, não apresenta sinais de decomposição à temperatura ambiente durante muitos anos. Nenhuma redução na doçura foi observada durante um período de aproximadamente 2 anos. A estabilidade a temperaturas elevadas é boa, embora tenha sido observada alguma decomposição após armazenamento a 408°C durante vários meses. A esterilização e a pasteurização não afetam o sabor do acessulfame de potássio.
O material a granel deve ser armazenado em recipiente bem fechado, em local fresco, seco e protegido da luz.
Incluído no banco de dados de ingredientes inativos da FDA para preparações orais e sublinguais. Incluído na lista canadense de ingredientes não medicinais aceitáveis. Aceito para uso na Europa como aditivo alimentar. Também é aceito para uso em determinados produtos alimentícios nos EUA e em vários países da América Central e do Sul, Oriente Médio, África, Ásia e Austrália.