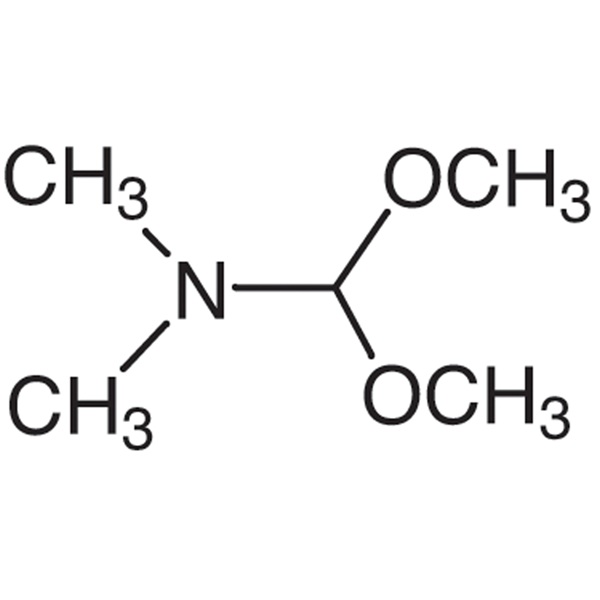
DMF-DMA CAS 4637-24-5 N,N-Dimetilformamida Dimetil Acetal Pureza >99,0% (GC) Venda quente de fábrica
Shanghai Ruifu Chemical é o fabricante líder de N,N-Dimetilformamida Dimetil Acetal (DMF-DMA) (CAS: 4637-24-5) com alta qualidade. Ruifu pode fornecer entrega em todo o mundo, preço competitivo, serviço excelente, quantidades pequenas e grandes disponíveis. Compre DMF-DMA, Entre em contato: alvin@ruifuchem.com
| Nome Químico | N,N-Dimetilformamida Dimetil Acetal |
| Sinônimos | DMF-DMA; 1,1-Dimetoxitrimetilamina; 1,1-Dimetoxi-N,N-Dimetilmetilamina; N-Dimetoximetil-N,N-Dimetilamina |
| Número CAS | 4637-24-5 |
| Status do estoque | Em estoque, produção em até toneladas |
| Fórmula Molecular | C5H13NO2 |
| Peso molecular | 119.16 |
| Ponto de ebulição | 102,0~103,0℃/720 mmHg (aceso.) |
| Gravidade específica (20/20) | 0,8940 a 0,8980 |
| Índice de refração n20/D | 1,3950 a 1,3980 (lit.) |
| Sensível | Sensível à umidade |
| Solubilidade | Miscível com a maioria dos solventes orgânicos |
| COA e MSDS | Disponível |
| Marca | Ruifu Química |
| Artigo | Especificações |
| Aparência | Líquido Transparente Incolor |
| Pureza/Método de Análise | >99,0% (GC) |
| Impurezas Totais | ≤1,00% |
| Espectro Infravermelho | Está em conformidade com a estrutura |
| Atenção | Evite água, que pode diminuir a pureza do produto |
| Padrão de teste | Padrão Empresarial |
| Uso | Intermediários Farmacêuticos |
Pacote: Garrafa, 25kg/Tambor, ou conforme necessidade do cliente.
Condição de armazenamento: Armazene em um recipiente bem fechado. Armazenar em local fresco, seco e bem ventilado, longe de substâncias incompatíveis. Proteja da luz e da umidade.
Envio: Entregue para todo o mundo por via aérea, pela FedEx / DHL Express. Fornece entrega rápida e confiável.

Códigos de risco
R11 - Altamente inflamável
R22 - Nocivo se ingerido
R36/37/38 - Irritante para os olhos, vias respiratórias e pele.
R36/38 - Irritante para os olhos e pele.
R20 - Nocivo por inalação
R20/21/22 - Nocivo por inalação, em contacto com a pele e por ingestão.
R10 - Inflamável
R52 - Nocivo para organismos aquáticos
Descrição de segurança
S16 - Manter afastado de fontes de ignição.
S26 - Em caso de contato com os olhos, lavar imediatamente com água em abundância e consultar um médico.
S36/37 - Use roupas e luvas de proteção adequadas.
S36/37/39 - Use roupas de proteção, luvas e proteção para os olhos/face adequados.
S33 - Tome medidas de precaução contra descargas estáticas.
S29 - Não despeje nos ralos.
S7/9 -
IDs ONU UN 3271 3/PG 2
GTK Alemanha 1
CÓDIGOS F DA MARCA FLUKA 21
TSCA Sim
Classe de perigo 3
Grupo de Embalagem II
Toxicidade LD50 por via oral em coelho: >5000 mg/kg
N,N-Dimetilformamida Dimetil Acetal (DMF-DMA) (CAS: 4637-24-5) tem uma ampla gama de aplicações, é um intermediário importante na síntese de compostos heterocíclicos, é também um bom reagente de metilação e agente desidratante de vinagre, especialmente como intermediários de síntese farmacêutica. DMF - DMA tem sido usado na esterificação metílica de ácido carboxílico. DMF-DMA é usado como intermediário na formação de derivados de piridina. DMF-DMA é utilizado para a derivatização de sulfonamidas primárias e ácido trifluoroacético. Também é utilizado na preparação de derivados de formamidina. É usado como reagente para n-dimetilaminometileno e ésteres metílicos. DMF-DMA é usado para catalisar o acoplamento de epóxidos com dióxido de carbono para preparar carbonatos cíclicos. DMF-DMA é um intermediário do Zaleplon (CAS: 151319-34-5).
Desde que Meenvin relatou a preparação de DMF-DMA (N,N-Dimetilformamida Dimetil Acetal) em 1956, o DMF-DMA tornou-se um reagente frequentemente utilizado em síntese orgânica.
DMF-DMA é amplamente utilizado na construção de anéis heterocíclicos de cinco ou seis membros em reações de fechamento de anel. DMF-DMA possui reação suave e alto rendimento, principalmente para compostos de alta resistência.
A estrutura geral dos compostos de amida acetal é a seguinte:
Os mais utilizados são DMF-DMA e DMF-DEA, o acetal amida é facilmente hidrolisado, podendo ser reações de esterificação, amidina, alquilação e ciclização.
O átomo de carbono central do DMF-DMA está conectado a três heteroátomos com grande eletronegatividade, o que o faz ter forte atividade eletrofílica. Sob a ação do ácido, o grupo alcóxi é fácil de sair e são obtidos íons positivos com atividade eletrofílica mais forte. A reação de DMF-DMA consiste principalmente em reação de metilação e reação de formação.
"One-carbon Syntheson" de DMF-DMA
Na reação de fechamento de loop envolvendo DMF-DMA, apenas um átomo de carbono no produto é frequentemente fornecido por DMF-DMA, então DMF-DMA pode ser considerado como um sintetizador de carbono.
Reação de esterificação DMF-DMA
A esterificação DMF-DMA permite que vários ácidos carboxílicos gerem facilmente ésteres alquílicos ou arílicos C1-20, e os subprodutos podem ser facilmente separados por destilação.
O ácido adípico e o DMF-DMA foram esterificados a 80 graus durante duas horas. O acetal amida é uma escolha ideal para esterificação de alguns ácidos carboxílicos com impedimento estérico ou baixa estabilidade.
Reação de amidinação DMF-DMA e proteção de aminas primárias
Os acetais de amida podem reagir não apenas com aminas primárias, mas também com amidas, carbamatos e sulfonamidas para formar ligações de hidrocarbonetos.
Tais como: 2, 4-dimetilanilina e DMF-DMA a 80 graus podem remover rapidamente o metanol para formar compostos de dimetamidina.
DMF -
Proteção de aminoácidos - 13 introdução de base de proteção comum, experiência de seleção de base de proteção, gama de uso, condições de introdução, compartilhamento de resumo de condições de remoção
DMF-DMA reage com grupos ativos metil e metileno para formar ligações duplas carbono-carbono
Fenilmetilação de DMF-DMA
Reações de compostos heterocíclicos em DMF-DMA
O acetal amida como doador único de carbono pode ser usado para sintetizar vários compostos complexos e substâncias naturais biomiméticas. Com acetais de amida podem ser sintetizados: 1,2,4 triazol, 1,2, 4 triazolona, derivados aminoheterocíclicos, pirimidina, pirimidina, indóis, piridina, quinolina, tiazol, oxazolona, isooxazol, 1,2, 4 - triazona, piranona, pirazina, pirazina e outras séries de derivados heterocíclicos de amônia, também podem ser sintetizados oxigênio, compostos heterocíclicos de enxofre.
De acordo com o tipo de reação química, a aplicação do amida acetal na síntese de compostos heterocíclicos pode ser dividida nos três aspectos a seguir.
(1): amida acetal e amina, amida, reação lipídica carbamato, geram uma variedade de anéis heterocíclicos
Reação de amidoacetal e amina para intermediário formamidina e, em seguida, reação de anel nucleofílico intramolecular para gerar vários heterociclos, ou formamidina e hidrazina, hidroxilamina, 1, 2, um ou dois haletos de alquil contendo dois grupos ativos de compostos mais cadeia de carbono longa e, em seguida, anel intramolecular.
Síntese de compostos heterocíclicos pela reação de acetais de amida e amidas, como a síntese de derivados de l,2,4 monotriazol. Primeiro, o acetal reage com a amida para formar N, N 'tritradil e, em seguida, forma anéis com fenilhidrazina para formar derivados de l, 2,4 monotriazol
Os acetais de amida reagem com ácido carbâmico ou acetato para formar anéis heterocíclicos contendo cloro. Intermediário diativo formado pela reação de um acetal amida com um éster aminoetílico: n.n-dimetil-n 'alquil-carboximetil formamidina, que reage com hidrazina ou hidrazina substituída. Por exemplo, para a preparação de 1,2,4 triazinona-6, a equação é mostrada abaixo. Se você reagir com um nitro-formato você obtém 1,2,4 triazolona-5.
Mecanismo de reação para formação de 1,2,4 triazolona-5
A composição de 1.2.4- triazolidina - 5 é duas etapas. Primeiro, carbamato de etila e acetais de diformaldeído DMF formam o intermediário Nn-dimetil-n-etoxi-formamidina. Em segundo lugar, o grupo amino da fenilhidrazina ataca o carbono da formamidina, que perde -N (CH3). Então a amônia no anel de benzeno próximo à fenilhidrazina ataca o carbono no grupo carbono, formando um ânion oxigênio, e o par solitário de elétrons no oxigênio desce, perde o grupo etoxi e produz 1,2, 4-triazolona-5.
(II) Preparação de compostos heterocíclicos pela reação de amida acetal e amida
Este é o método de síntese de impurezas mais relatado nas últimas décadas. A ação do amida acetal é equivalente ao reagente de Grignard, mas a condição de reação do amida acetal é simples e suave.
Amida acetal tem dois grupos ativos, alta reatividade e metil ativo, reação de metileno para formar intermediários de amidina, pode ser reação adicional, fechamento de anel e reagente de Grignard e reação de metileno, apenas alongando a cadeia de carbono, não pode ser reação adicional. Por exemplo, síntese de derivados de furanocrona.
(3): amida acetal e hidroxila, reação de composto sulfidrila para gerar oxigênio, compostos heterocíclicos de enxofre
A síntese de furohutanona acima é um bom exemplo da geração de acetal de derivados de enamina e grupo hidroxila pela separação do pólo endolateral, resultando em heteramina contendo oxi-. Outro exemplo: catecol e DMF -- O DMA forma anéis contendo oxigênio na presença de diclorometano.
A reação do DMF -- DMA e o - mercaptoanilina podem produzir anel heterocíclico contendo enxofre, a fórmula da reação é a seguinte
Estudo de caso da reação de fechamento do anel DMF-DMA e reação pessoal
(1) Síntese de indol Batcho-Leimgruber
Preparação de vários derivados Vindol a partir do o-nitrotolueno.
Mecanismo de reação
Em primeiro lugar, dimetilformamida dimetilacetal, os íons negativos do grupo metoxi deixam de produzir um intermediário mais reativo. É atacado por carboânions formados pela desprotonação do onitrotolueno metil hidrogênio e perde o metanol para obter a enilamina mencionada acima. O produto desta etapa, enamina, se assemelha a um alceno com substituintes retiradores de elétrons e doadores de elétrons ligados em ambos os lados (a olefina push - pull é fortemente polar e muitas vezes vermelha escura devido à grande faixa de conjugação na molécula. Na segunda etapa da reação, o grupo nitro é reduzido a um grupo amino, seguido de ciclização e eliminação para obter o produto final.
(2) Imagens compostas de derivados de piridina
(3) Síntese de derivados de pirazol