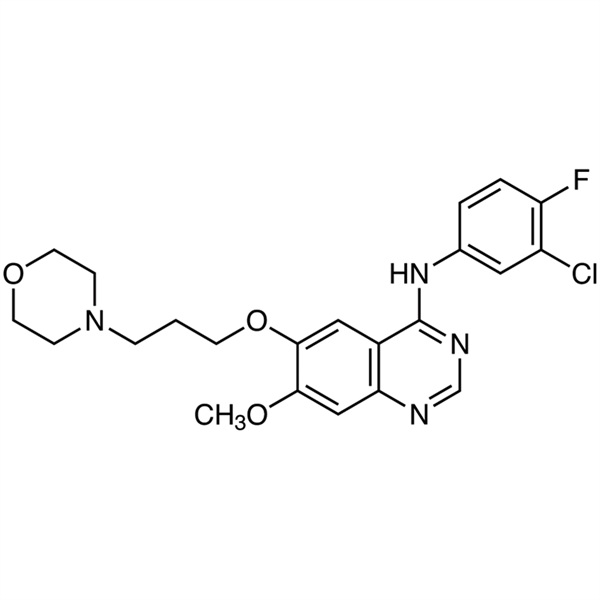
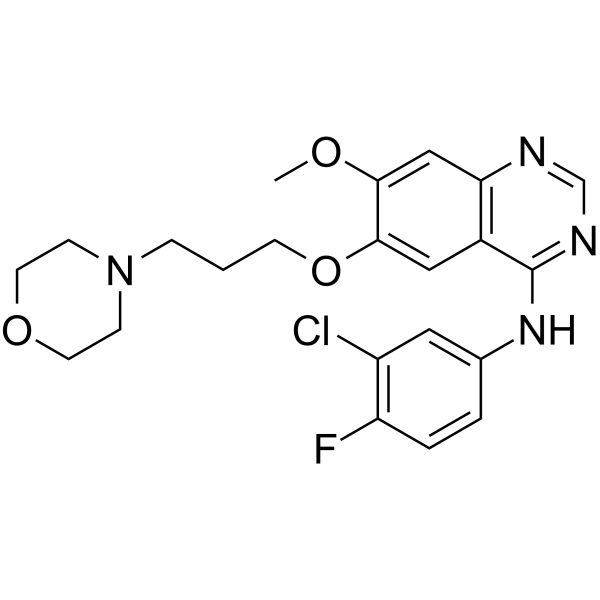
Gefitinibe CAS 184475-35-2 Pureza >99,5% (HPLC)
Shanghai Ruifu Chemical Co., Ltd. é o fabricante líder de Gefitinibe (CAS: 184475-35-2) com alta qualidade. A Ruifu Chemical pode fornecer entrega em todo o mundo, preço competitivo, serviço excelente, quantidades pequenas e a granel disponíveis. Compre Gefitinibe e intermediários, Entre em contato: alvin@ruifuchem.com
| Nome Químico | Gefitinibe |
| Sinônimos | Base Livre de Gefitinibe; Iressa; ZD1839; ZD-1839; N-(3-Cloro-4-Fluorofenil)-7-Metoxi-6-(3-Morfolinopropoxi)quinazolina-4-Amina; N-(3-Cloro-4-Fluorofenil)-7-Metoxi-6-[3-(4-Morfolinil)propoxi]-4-Quinazolinamina |
| Status do estoque | Em estoque, produção comercial |
| Número CAS | 184475-35-2 |
| Fórmula Molecular | C22H24ClFN4O3 |
| Peso molecular | 446,91 g/mol |
| Ponto de fusão | 194,0 a 198,0 ℃ |
| Densidade | 1,322±0,06 g/cm3 |
| Solubilidade | Insolúvel em água. Solúvel em DMSO |
| Temperatura de armazenamento. | Temperatura ambiente |
| Envio | Ambiente |
| COA e MSDS | Disponível |
| Origem | Xangai, China |
| Categorias de produtos | API (Ingrediente Farmacêutico Ativo) |
| Marca | Ruifu Química |
| Itens | Padrões de Inspeção | Resultados |
| Aparência | Branco a desativado - Pó branco | Cumpre |
| Perda na secagem | <0,50% | 0,13% |
| Resíduos na ignição | <0,20% | 0,06% |
| Impureza Única | <0,10% | 0,09% |
| Impurezas Totais | <0,50% | 0,20% |
| Metais Pesados (Pb) | ≤10ppm | <10 ppm |
| Pureza do Gefitinibe | >99,5% (HPLC) | 99,80% |
| Espectro Infravermelho | Consistente com a Estrutura | Cumpre |
| Espectro de RMN 1H | Consistente com a Estrutura | Cumpre |
| Conclusão | O produto foi testado e está em conformidade com as especificações fornecidas | |
Pacote: Frasco fluorado, saco de papel alumínio, 25kg/tambor de papelão ou conforme necessidade do cliente.
Condição de armazenamento: Manter o recipiente bem fechado e armazenar em local fresco, seco e bem ventilado, longe de substâncias incompatíveis. Proteja da luz e da umidade.
Envio:Entregue para todo o mundo por via aérea, pela FedEx / DHL Express. Fornece entrega rápida e confiável.
Não é para uso em humanos. Não deve ser usado em diagnóstico ou terapêutica. Apenas para uso em pesquisa in vitro.
Nenhum dos produtos será fornecido a países onde isso possa entrar em conflito com as patentes existentes. No entanto, a responsabilidade final é do Comprador.
Como comprar? Entre em contatoAlvin Huang: sales@ruifuchem.com ou alvin@ruifuchem.com
15 anos de experiência?Temos mais de 15 anos de experiência na fabricação e exportação de uma ampla variedade de intermediários farmacêuticos ou produtos químicos finos de alta qualidade.
Principais mercados? Vender para o mercado interno, América do Norte, Europa, Índia, Coréia, Japão, Austrália, etc.
Vantagens? Qualidade superior, preço acessível, serviços profissionais e suporte técnico, entrega rápida.
Qualidade Garantia? Sistema de controle de qualidade rigoroso. Equipamentos profissionais para análise incluem NMR, LC - MS, GC, HPLC, ICP - MS, UV, IR, OR, K.F, ROI, LOD, MP, Claridade, Solubilidade, teste de limite microbiano, etc.
Amostras? A maioria dos produtos fornece amostras grátis para avaliação de qualidade. O custo de envio deve ser pago pelos clientes.
Auditoria de Fábrica? Auditoria de fábrica bem-vinda. Por favor, marque uma consulta com antecedência.
Quantidade mínima? Sem quantidade mínima. Pedidos pequenos são aceitáveis.
Prazo de entrega? Se estiver em estoque, entrega garantida em três dias.
Transporte? Por expresso (FedEx, DHL), por via aérea, por via marítima.
Documentos? Serviço pós-venda: COA, MOA, ROS, MSDS, etc.
Síntese Personalizada? Pode fornecer serviços de síntese personalizados para melhor atender às suas necessidades de pesquisa.
Condições de pagamento? A fatura pró-forma será enviada primeiro após a confirmação do pedido, juntamente com nossos dados bancários. Pagamento por T/T (Transferência Telex), PayPal, Western Union, etc.
| Descrição de segurança | 24/25 - Evite o contato com a pele e os olhos. |
| Código HS | 2934999099 |
Gefitinibe (CAS: 184475-35-2) é um medicamento terapêutico antitumoral altamente específico desenvolvido pela AstraZeneca, Reino Unido. É o primeiro medicamento de alvo molecular para o tratamento do câncer de pulmão de células não pequenas. Atua inibindo seletivamente a via de transdução de sinal do receptor tirosina quinase do fator de crescimento epidérmico (EGFR - TK). O fator de crescimento epidérmico (EGF) é um polipeptídeo com massa molecular relativa de 6,45 × 103, que pode se combinar com o receptor do fator de crescimento epidérmico (EGFR) na membrana da célula alvo para produzir efeitos biológicos. EGFR é um receptor do tipo tirosina quinase (TK). Quando se liga ao EGF, pode promover a ativação da TK no corpo receptor, resultando na autofosforilação dos resíduos de tirosina do receptor, fornecendo sinais de divisão contínua às células, causando proliferação e diferenciação celular. O EGFR é abundante em tecidos humanos e altamente expresso em tumores malignos. Ao bloquear a via de sinalização do EGFR na superfície celular, o gefitinibe impede o crescimento tumoral, a metástase e a angiogênese, e pode induzir a apoptose das células tumorais. Em agosto de 2002, o gefitinibe foi comercializado pela primeira vez no Japão como tratamento de primeira linha para câncer de pulmão de células não pequenas, sob o nome comercial Iressa. Em maio de 2003, a Food and Drug Administration dos EUA aprovou o gefitinibe como monoterapia de terceira linha para pacientes com câncer de pulmão de células não pequenas avançado que foram ineficazes com medicamentos anticancerígenos à base de platina e quimioterapia com docetaxel. Atualmente, foi aprovado pela Austrália, Japão, Argentina, Singapura e Coreia do Sul para o tratamento do câncer avançado de pulmão de células não pequenas. Em 28 de fevereiro de 2005, a Administração de Alimentos e Medicamentos da China aprovou o gefitinibe para o tratamento de câncer de pulmão de células não pequenas (NSCLC) localmente avançado ou metastático que já havia recebido quimioterapia. Atualmente não está aprovado para uso como terapia de primeira linha para NSCLC avançado. Em 1º de julho de 2009, a Agência Europeia de Medicamentos aprovou oficialmente o gefitinibe para tratamento de primeira linha, segunda linha e terceira linha de câncer de pulmão de células não pequenas localmente avançado ou metastático com mutações no gene EGFR em adultos.